USP官方已确认!重组C因子爱“鲎”之路,迎来内毒素检测新突破
来源:瀚海生物市场中心 时间:2024-08-22 作者:瀚海新酶 浏览量:363
2024 年 7 月 26 日,美国药典委员会微生物学专家委员会已批准第<86>章:细菌内毒素检测,允许使用非动物源性的重组 C 因子法 (rFC) 进行内毒素检测,最终文本将于 2024 年 11 月发布,并将于 2025 年 5 月正式生效
2021 年 6 月生效的《欧洲药典》2.6.32 章节中明确重组 C 因子法作为细菌内毒素的替代方法,使用重组 C 因子法进行内毒素检测不需要经过方法的验证,使用重组 C 因子法进行细菌内毒素检查的方法与现行内毒素检查法的方法相同

中国自 2012 年就开始关注重组 C 因子法,2016 年国家药典委员会立项 “细菌内毒素检查法的新方法研究”,由中国食品药品检定研究院协同山东省食品药品检验研院、江苏省食品药品监督检验研究院、山西省食品药品检验所对重组 C 因子法进行了系统的方法学验证和品种适用性研究,在准确度、精密度、耐用度、线性和范围、检测限、专属性等方面进行了评价,并研究了品种应用范围,确定该方法可作为现有细菌内毒素检查法的替代方法
《中国药典》2020 版,在 9251 细菌内毒素检查法应用指导原则中列出了重组 C 因子法。

重组C因子法,越来越“重要”
各国药典陆续推荐使用重组 C 因子法 (rFC) 进行内毒素的检测,因为细菌内毒素检测是确保无菌药品质量和安全的关键环节之一。
传统的鲎试剂检测方法,需要用到国家保护动物鲎,属于动物来源且存在不可持续的问题。随着 2021 年中国将鲎列为国家二级重点保护野生动物,采用无动物来源的重组 C 因子法 (rFC) 替代传统鲎试剂检测内毒素,是一种可持续性环保的解决方案。
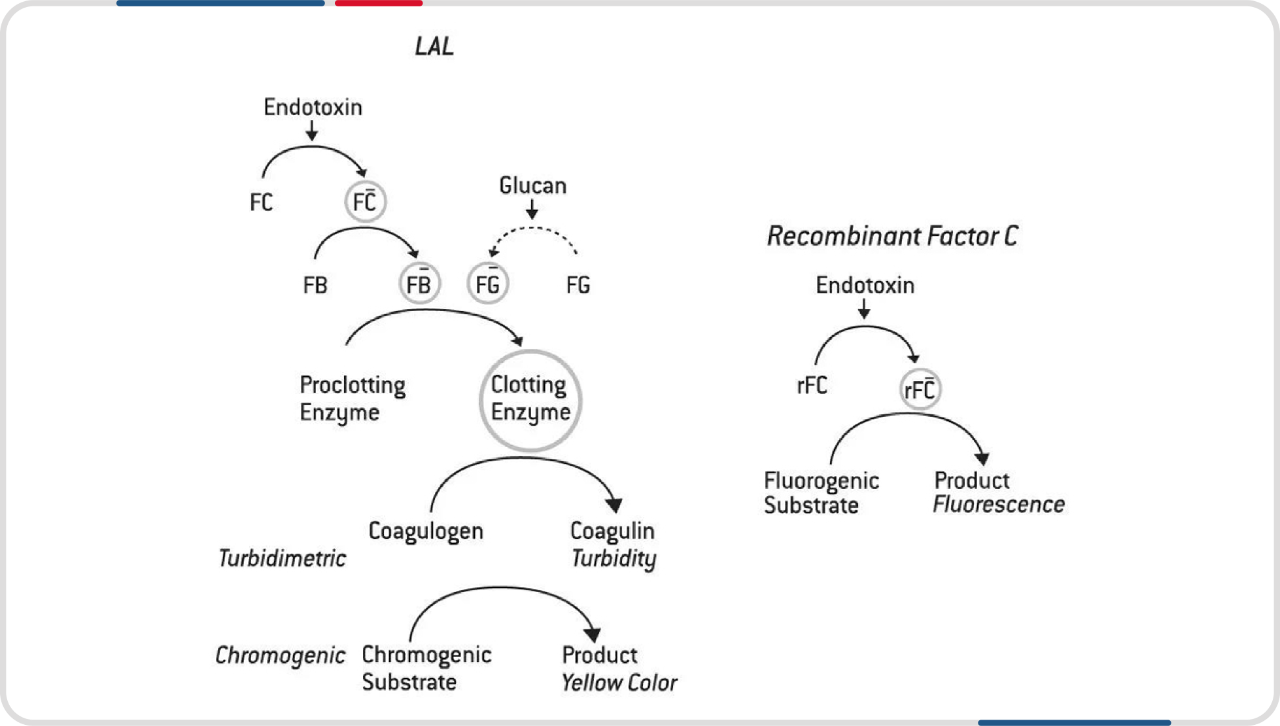
重组 C 因子法 (rFC) ,使用单一的蛋白质 C 因子作为活性成分参与反应,被内毒素活化的 C 因子将荧光底物裂解,产生荧光复合物,通过定量检测荧光复合物来量化细菌内毒素。能有效避免因 G 因子的旁路干扰而产生的假阳性,能更加精确的检测出内毒素含量,保障注射制品的生物安全性。
以 “逸” 待 “牢”
瀚海新酶重组 C 因子内毒素检测试剂盒,是以基因重组的方式表达 C 因子重组蛋白,通过内毒素结合并激活重组 C 因子,再切割荧光底物获得游离的荧光基团,荧光基团的释放与内毒素的浓度呈正比,从而定量检测内毒素含量。
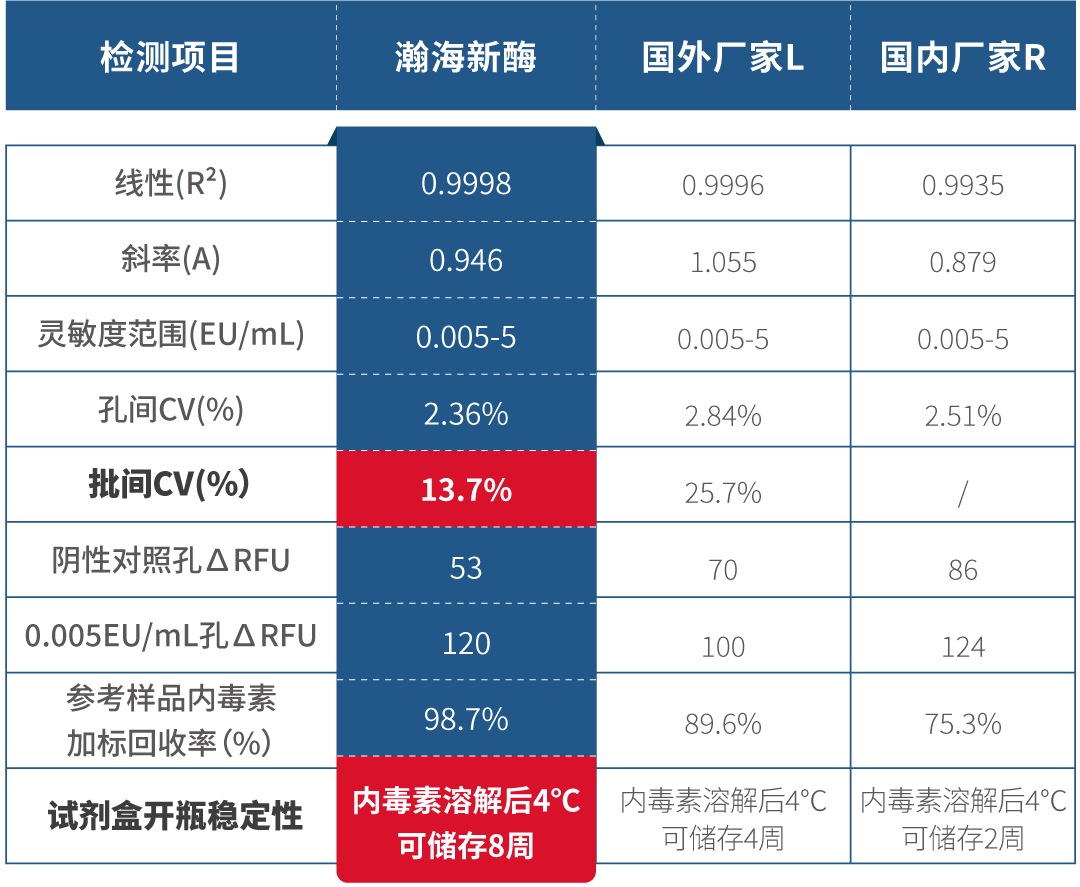
与鲎试剂相比,重组 C 因子内毒素检测法具有:更好的特异性、专属性、精密度、准确度、线性范围及定量限,是内毒素检测的未来主流方法。
01特异性
重组技术消除了传统鲎试剂中 G 因子旁路的干扰,可避免结果出现假阳性。
02 可持续性
消除了对动物源试剂的依赖,符合3R (优化、减少、替代) 及生态可持续性。
03 稳定性
更好的批次稳定性,标准品 4℃ 保存可长达 60 天。
04 解决方案
针对各类回收率异常样本,可提供多种内毒素解遮蔽方案。
05 简便性
一次性提供标准品和可拆卸酶标板,提供 48T 和 96 规格





 USA
USA








